研究発表における研究倫理等申告について
▷ ページを更新する 研究内容に応じて、臨床研究法あるいは「人を対象とする医学系研究に関する指針」等の医学研究に関する指針を遵守する必要があります。
日本呼吸ケア・リハビリテーション学会では、今学術集会より、発表演題について、研究・倫理に関する規範に基づいて適切に審査を受けていることを申告いただくことになりました。報告・研究の内容によっては、施設の倫理審査会等での審議承認は不要ですが、研究倫理申告が必要な場合がありますのでご留意ください。 用語に関しては「人を対象とする生命科学・医学系研究に関する倫理指針」(令和3年3月23日公布)をご参照ください。 申告にあたりまして下記に記載のフローチャートで要否をご確認ください。
ただし、今回の学術集会では、倫理委員会での審査が必要な発表演題の場合でも、自施設に倫理委員会がなく、承認を得ることが難しい場合に限って、倫理委員会承認がない発表も受け付けます。 |
申告事項
1.人を対象とする研究ですか?
□はい
□いいえ
「いいえ」と回答された場合、以下の申告は不要です。
2.ご発表の演題は以下のいずれかに該当しますか?(複数回答可)
□9例以下をまとめた研究性のない症例報告.
□傷病の成因・病態の理解、傷病の予防・診断・治療方法の改善、有効性・安全性の検証を通じて、人の健康の保持増進または傷病からの回復・生活の質の向上に資する知識を得ることを目的としない報告等.
(例 ①単に治療方法の紹介、教育・トレーニング方法の紹介、②機関の医療体制や受診率向上の取り組みに関する紹介)
□論文や公開されているデータベース、ガイドラインのみを用いた研究.
□既に学術的な価値が定まり、研究用として広く利用され、かつ、一般に入手可能な試料・情報を用いた研究.
□既に匿名化されている試料・情報を用いた研究.
(特定の個人を識別できない状態に加工され、自他問わず対応表がどこにも存在しないものを用いた研究.例:メタアナリシスなど.但し、体細胞由来のゲノムデータ解析は除く)
□既に作成されている匿名加工情報または非識別加工情報を用いた研究.
□法令に基づく研究.
(臨床研究法、再生医療等安全性確保法は除く)
□人体から分離した細菌、カビ、ウイルス等の微生物の分析等を行うのみで、人の健康に関する事象を研究の対象としない研究.
□動物実験や一般に入手可能な細胞(iPS 細胞、組織幹細胞を含む)を用いた基礎的研究.
□海外で実施された研究.
(但し、実施した国の規定は遵守していることが必要.研究対象となった試料・情報が日本のものは除く)
上記のいずれかに該当する場合は、以下の申告は不要です。
3.ご発表の演題は以下のいずれかに該当しますか?
□既存の試料・情報を用いる観察研究.
(通常診療の情報や診療で採取された生体試料の余剰分を用いるもの等、通常の診療行為に影響を与えないが、前向き後ろ向き研究であることを問わない)
□研究目的で新たに情報のみを取得する観察研究であって、侵襲を伴わない研究.
(心電図、体表US検査、心的侵襲のないアンケートを実施するものが含まれる)
□研究目的で新たに情報を取得する際に侵襲または軽微な侵襲を伴う観察研究.
(通常の診療行為に影響を与えないが、研究目的にX線撮影、CT等を実施する研究が含まれる)
□研究目的で新たに情報に加えて試料を取得する観察研究.
(通常の診療行為に影響を与えないが、研究目的にCT、採血(通常診療に加えて量を追加する場合も含む)、組織採取等を追加する侵襲あるいは軽微な侵襲を伴うものと、排泄物の採取など侵襲を伴わないものが含まれる)
□「臨床研究法」の適用されない介入研究.
(体外診断薬を用いた介入研究、医療手技や手術方法の評価を行う研究が含まれる)
□特定臨床研究以外の臨床研究(「臨床研究法」の遵守努力義務の対象となる研究).
(既承認の医薬品・医療機器等を用いてそれらの有効性・安全性を評価する介入研究で、関連する企業から資金提供が無い研究が該当する)
□特定臨床研究(「臨床研究法」の遵守義務の対象となる研究).
(未承認・適応外の医薬品・医療機器等を用いる研究、または企業から資金提供を受ける介入研究が該当する)
※特定臨床研究に含まれない未承認薬・適応外の医療に関する報告について、1例の症例報告であっても施設内の倫理審査委員会等での承認をお願いします.
□遺伝性疾患に関わる報告・研究.
□その他、以下に当てはまる研究.
・再生医療等安全性確保法に該当する研究.
・ヒトの遺伝子治療に関する研究.
上記のいずれかに該当する場合は、各研究が適用される規制に基づく委員会の審査が必要となります. 以下の申告にお進みください。
ただし、今回の学術集会では、委員会の審査が必要な場合でも、自施設に倫理委員会がなく、承認を得ることが難しい場合に限って、倫理委員会承認がない発表も受け付けます。 |
・特定臨床研究に関するQ&Aについては、厚生労働省:臨床研究法の施行等に関するQ&A;確定版1 QA(統合版) (mhlw.go.jp)を参照ください。
4. ご発表予定の演題は、適用となる研究・倫理に関する規範に基づき、研究・倫理審査委員会等で審議され、承認されていますか?
□はい
□いいえ (審議中)
□いいえ (審議済、非承認)
□該当せず
「該当せず」と回答された場合、その理由を下記に簡潔に記載してください。
以上で、倫理申告は終了です。
「はい」の申告につきましては演題発表が可能です。
「いいえ」(審議中)の申告におきましては、学術集会開催日の前日までに承認された場合に限り 演題発表が可能となりますので、必ず承認を得るようお願いします。
「いいえ」(審議済、非承認)につきましては、演題発表ができません。
登録した場合は取下げて頂くことになります。
「該当せず」の申告につきましては、その理由を審査し、不適切な場合は取下げていただくことになります。
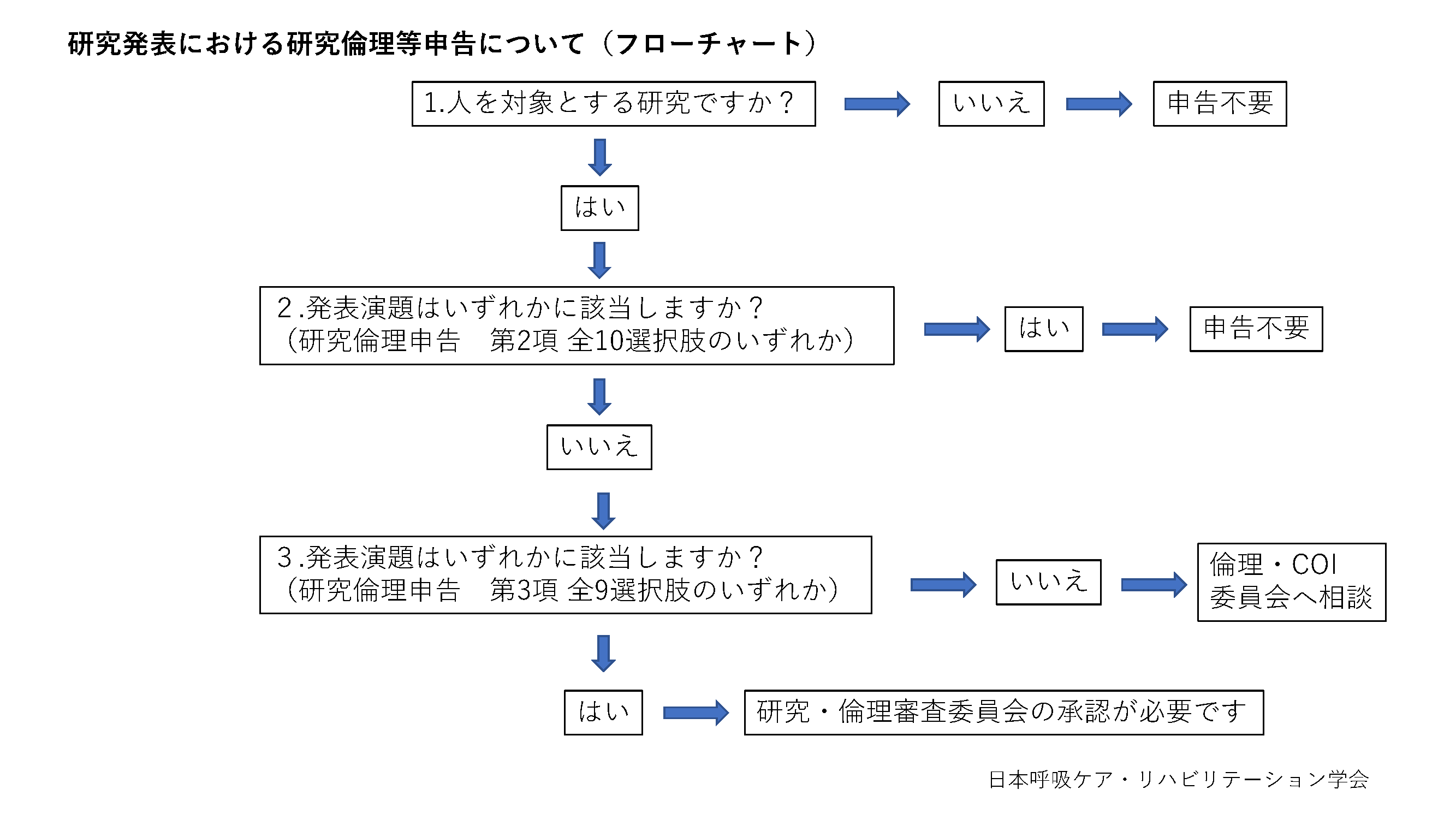
<フローチャート>