B. これまでの成果と今後の展望
5. 細胞死に直結する分子異常の解析
(ア) 核の異常
- ① AR2マウス運動ニューロンの核にはCa2+の流入依存性に大きな空胞ができている24→ 核膜に異常があるだろう、この異常は細胞死に繋がる可能性がある。
- ② 正常な核膜は核と細胞質の分子移動を制限しており物質の通過は核膜孔複合体Nuclear Pore Complex (NPC)を通じて行われる。
- 1. 核-細胞質の物質輸送:核→細胞質(RNA)、細胞質→核(タンパク RBP)
- 2. 輸送システム:NPC、Importin、Exportin、など
(イ) AR2マウス運動ニューロンの核膜異常25
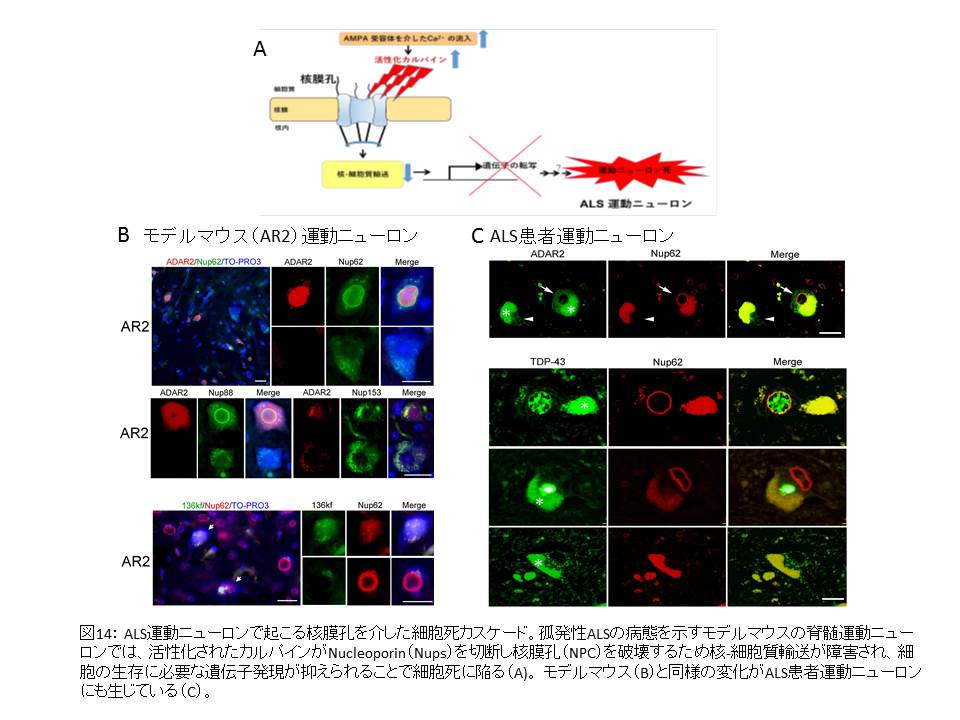 図14
図14
- ① NPCが破壊されている:Nupsの免疫活性消失
- ② 核・細胞質輸送に関わる分子の異常:Importin、Exportinの免疫活性消失
- ③ 核膜の構造的破壊:Lamin B(核の裏打ちタンパク)の消失
(ウ) カルパインがNups(NPC構成タンパク)を切断
- ① Nupsはカルパインにより特異的に分解される
- ② (イ)はカルパインが活性化したADAR2 欠損運動ニューロンに観察される
- ③ ADAR2活性低下に依るAMPA受容体からのCa2+流入増大がその原因。TDP-43病理の原因でもある(前項(ウ))
(エ) 核・細胞質物質輸送の破綻と細胞死
- ① 運動ニューロンでの転写活性低下
- 1. リン酸化RNA Polymerase IIの発現している運動ニューロン数が減少
- ② 運動ニューロンの生存に必要な遺伝子発現が低下=細胞死の原因
(オ) ALSの運動ニューロン25
- ① 孤発性ALSではAR2マウスと同様のNPC変化がみられる
- ② NPCの異常はTDP-43病理と共存している
- ③ すなわち、ADAR2 活性が低下し、カルパインが活性化している運動ニューロンに観察される
- ④ C9ORF72関連ALSでも核-細胞質の物質輸送障害が病因的意義を持つことが報告されている
(カ) これらのことから、ADAR2発現低下→未編集型GluA2発現→Ca2+透過性AMPA受容体発現→カルパインの活性化→TDP-43病理、と平行して
- ① →NPC破綻→遺伝子発現変化→運動ニューロンの生存に必須な遺伝子発現の低下→緩徐な細胞死と言う分子カスケードが考えられる。
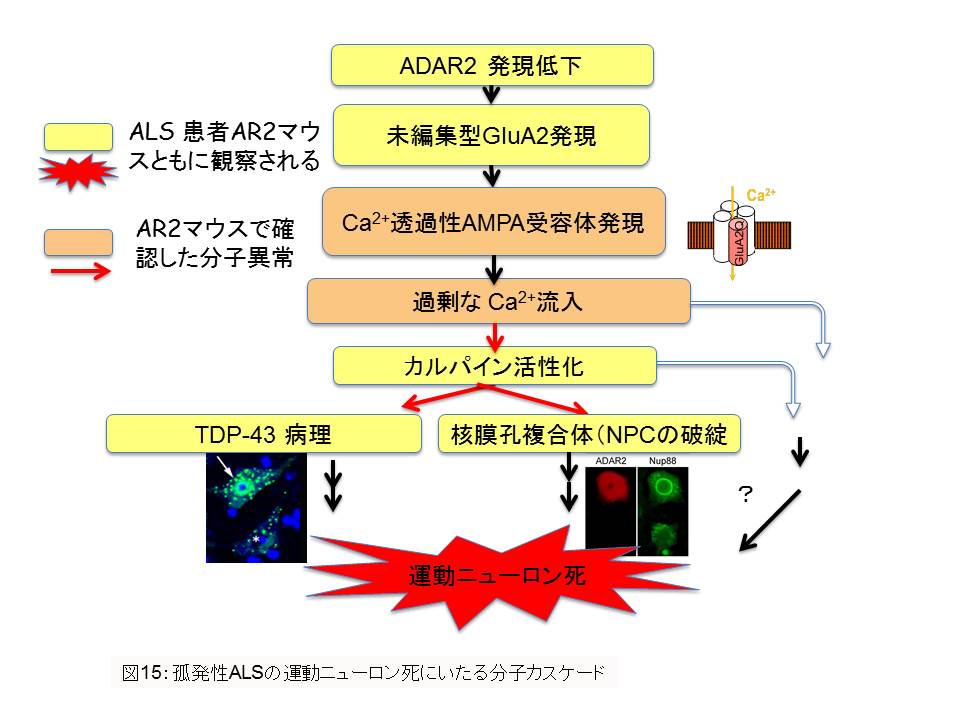 図15
図15
(キ) ADAR2 発現低下、未編集型GluA2の発現は孤発性ALSのみならず、一部の遺伝性ALSの運動ニューロンにも確認されている。
- ① FUS関連ALS:FUSP525L変異26
- ② G4C2反復伸長27
(ク) ADAR2発現低下の分子メカニズムを解析している。