研究代表者:立川 正憲(東北大学大学院 薬学研究科 薬物送達学分野 准教授)
てんかんの薬物治療において、病態の進行に伴う薬剤感受性の低下は、治療成績を増悪させる深刻な問題である。その原因の一つは、病巣部位の血液脳関門Blood-brain barrier (BBB)における薬物輸送機能の可塑的変化であるとの説が有力である。これは神経活動の異常亢進とBBB機能が、密接に連関していることを強く示唆している。特にアストロサイトは、解剖学的に脳血管に接しており、様々な液性因子を介して、BBBの機能を制御していることが明らかにされてきた。しかし、てんかん病態におけるBBBの機能変化に対して、アストロサイトの果たす役割は不明なままである。そこで本研究は、定量プロテオミクスと薬物輸送速度論を用いて、「神経活動-BBB機能連関におけるアストロサイトの役割」を解明し、新たな”glio-vascular coupling”の概念を提唱することを目的とし、薬物治療耐性克服への突破口を開く。
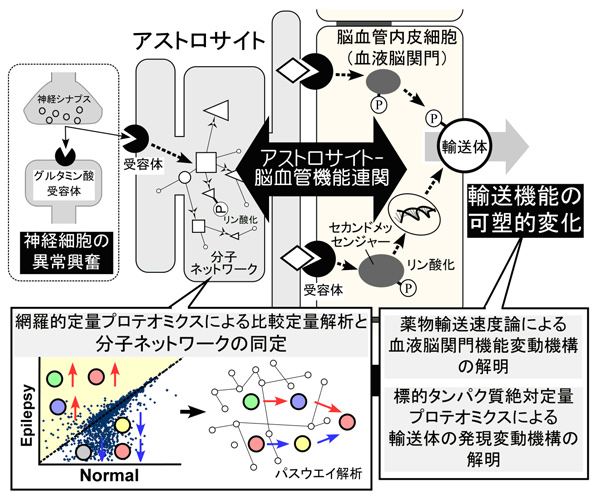
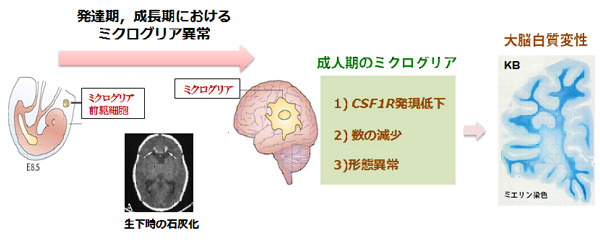
研究代表者:池内 健(新潟大学 脳研究所 遺伝子機能解析学 教授)
ミクログリアは発生・分化から成熟期に至るまで脳の恒常性の維持に重要な役割を果たしている。そのようなミクログリアの機能に着目しながら、本課題ではミクログリアの機能異常が大脳白質変性の原因となる「一次性ミクログリア病」について研究を行う。一次性ミクログリア病の例として、CSF-1R変異を原因とする神経軸索スフェロイド形成を伴うびまん性白質脳症(HDLS)がある。私たちは現在までに、HDLSはCSF-1Rシグナルの減弱を原因とすること、患者脳ではミクログリアの数が減少し形態異常を呈することを明らかにした。最近、HDLS患者脳には特徴的な脳内微小石灰化が生じることを見出した。この石灰化は胎生期にミクログリアが集簇する部位に認められ、この変化は幼少期に検出できる。つまり、疾患としては成人期に発症するが、ミクログリアの異常は胎生期まで遡る可能性がある。長期のミクログリアの変調が大脳白質変性を誘導する分子病態を明らかにしていきたい。
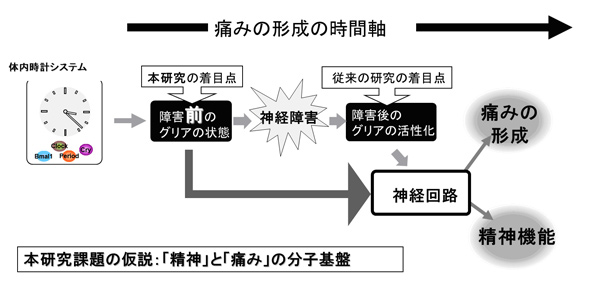
研究代表者:宝田 剛志(岡山大学大学院 医歯薬学総合研究科 組織機能修復学分野 准教授)
グリア病である神経障害性疼痛は、精神的ストレスや精神疾患との関連性が臨床上指摘されているが、この「精神と疼痛(痛み)」の関連性(連関)の分子基盤は未解明である。我々の解析結果より、睡眠障害等の精神疾患との関連性が深い体内時計システムが破綻したマウスでは、脳・脊髄組織でのアストロサイトの異常活性化が認められた。同マウスにて行動学的解析を実施した結果、多動といった精神行動異常が観察されただけでなく、神経障害性疼痛モデルを実施した結果、障害時における疼痛(アロディニア)に異常が認められた。本研究では、従来の疼痛研究の対象を変えて障害前のグリアに注目することで、「グリアネットワークの破綻」を、単一個々の精神神経疾患ではなく、「精神と痛み」連関メカニズムにおける共通の中間表現型として捉え、「体内時計によるグリアネットワークの制御」という観点から、「精神と痛み」連関の分子メカニズムを明らかとする。
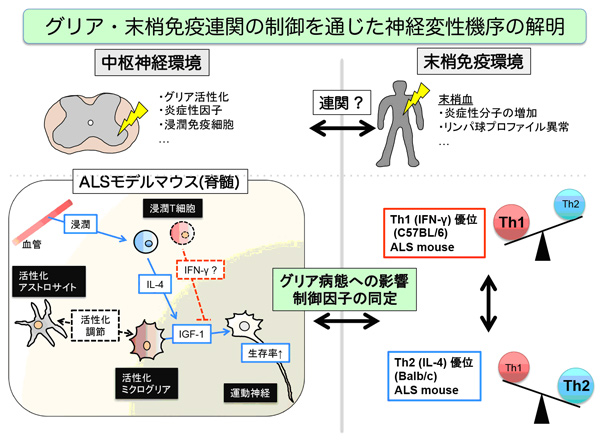
研究代表者:山中 宏二(名古屋大学 環境医学研究所 病態神経科学分野 教授)
運動神経変性を特徴とする神経変性疾患である筋萎縮性側索硬化症(ALS)において、グリア細胞がその病態に積極的に関与することを示し、「非細胞自律性」の神経変性という概念を提示してきた。近年、この概念は脊髄に浸潤する免疫細胞にも広がり、神経変性モデルマウスでは、中枢神経へ浸潤した免疫細胞がミクログリアの活性化を変容し、積極的に病態に関与しうることが示唆されている (Endo et al. Cell Rep, 2015)。一方で、ALS患者やALSマウスの病態が進行するにつれて、末梢血における免疫・炎症関連分子や免疫細胞の発現プロファイルが変化することが報告されているが、グリア病態への関与は未解明である。本研究では、末梢免疫環境の変容によるALSのグリア病態の制御に関与する細胞や分子を同定して、末梢免疫・中枢グリア連関のメカニズムを解明することを目標とする。
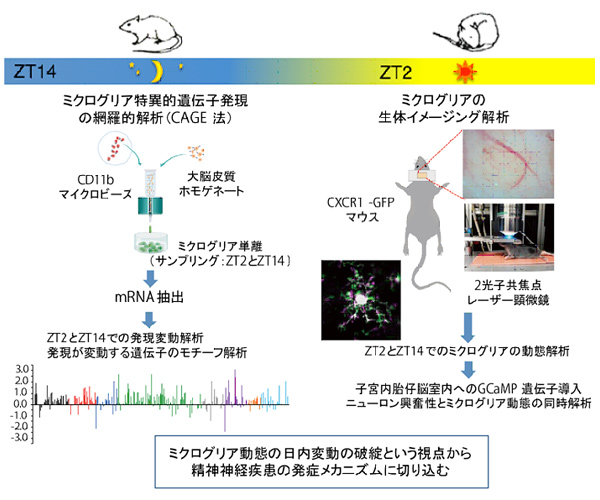
研究代表者:中西 博(九州大学歯学研究院 口腔機能分子科学分野 教授)
ミクログリアがClock-Bmal1を主軸とした分子時計を内在することを明らかにし、その制御下にあるミクログリア特異的分子(P2Y12受容体ならびにカテプシンS)の遺伝子発現量の日内変動が皮質ニューロンのスパイン密度ならびにシナプス活動の日内変動に関与することを突き止めた(Hayashi et al, Sci Rep 2013)。さらに蛍光生体イメージングにより脳内感染させた歯周病菌に向けたUDP—P2Y6受容体を介したミクログリアの突起伸展反応は日内変動を示すことを明らかにした(Takayama et al, Sci Rep 2016)。これらの結果よりミクログリアにおける機能分子発現の日内変動は、ミクログリアの動態を制御している可能性が考えられる。そこで本研究はミクログリアの動態の日内変動とその分子的基盤を明らかにし、ミクログリアの動態の日内変動破綻という視点から精神神経疾患の発症メカニズムに切り込む。
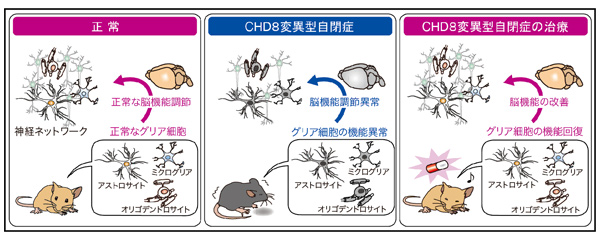
研究代表者:西山 正章(金沢大学 医薬保健研究域医学系 組織細胞学 教授)
グリア細胞の機能異常は不完全な神経回路形成を引き起こし、自閉症などの精神疾患の発症に寄与することが示唆されている。近年、自閉症患者における大規模な原因遺伝子探索によってクロマチンリモデリング因子CHD8が最も有力な自閉症原因遺伝子候補として同定された。われわれは自閉症患者のCHD8変異を再現したモデルマウスを作製し行動解析を行ったところ、予想通り自閉症様の行動異常が観察された (Nature, in press)。さらにCHD8は神経細胞だけでなくグリア細胞にも発現が認められ、予備的な研究によってCHD8がオリゴデンドロサイトの分化に必須であることが判明した。そこで、本研究ではCHD8によるグリア細胞の機能制御メカニズムを解明すると共に、グリア細胞の機能異常による神経回路恒常性の破綻が自閉症の病態形成にどのように関与しているのかを明らかにすることによって、疾患治療への応用を目指す。
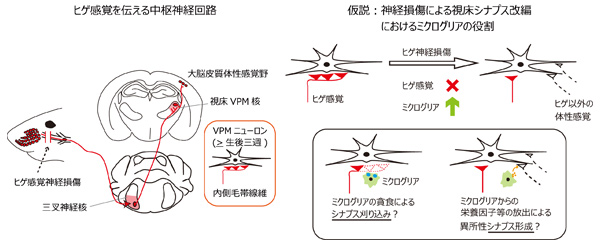
研究代表者:宮田 麻理子(東京女子医科大学医学部 生理学(第一)講座 教授)
末梢神経の損傷は、その投射路の上位中枢で神経回路の改編を引き起し、これは脳内マップの改変や幻肢痛にも深く関わることが知られている。我々は、視床VPM核へのヒゲ由来の上行性の内側毛帯線維シナプスを他と識別化することで、ヒゲ感覚神経を損傷したマウスのVPMにおいてヒゲ由来の内側毛帯線維シナプスが弱化し(シナプス刈り込み)、ヒゲ以外の体幹や下顎由来の内側毛帯線維シナプスが、ヒゲ領域ニューロンに異所性シナプスをつくることを見いだした。ミクログリアには、シナプス貪食と神経栄養因子等の放出による神経伸長作用の二つの機能があるとされている。本研究では、視床のシナプス刈り込み・異所性シナプス形成といった神経損傷によって引き起こされる二種類のシナプス改編機構に対し、ミクログリアが特異的に作用するかを検討し、それにより体部位マップ変化や異所痛行動にミクログリアが与える影響を明らかにする。
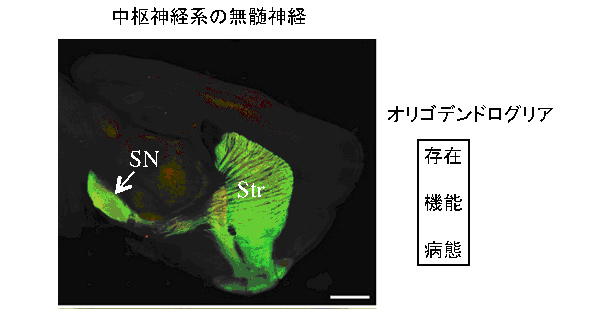
研究代表者:貫名 信行(同志社大学大学院 脳科学研究科 認知記憶加齢部門 教授)
中枢神経系における無髄神経の分布は意外なほど未解明である。我々は最近大脳基底核線条体投射線維が無髄神経からなっていることを報告した(Miyazaki et al Nat Commun2014)。オリゴデンドログリアは有髄では髄鞘形成を行うが、無髄神経系ではどのような存在様式であるかも十分知られていない。そこで本研究では応募者が同定している無髄神経系のマーカーを用いて中枢神経系の様々な部位での無髄神経に関してオリゴデンドログリアとの関連を有髄神経系と比較しながら明らかにする。また無髄神経がオリゴデンドログリアとの間でシグナル伝達を行っているのかどうか等、無髄神経とオリゴデンドログリアとのクロストークについても検討する。さらに多系統萎縮症などオリゴデンドログリアの病変を生ずる疾患において無髄神経の領域での病変を検討する。