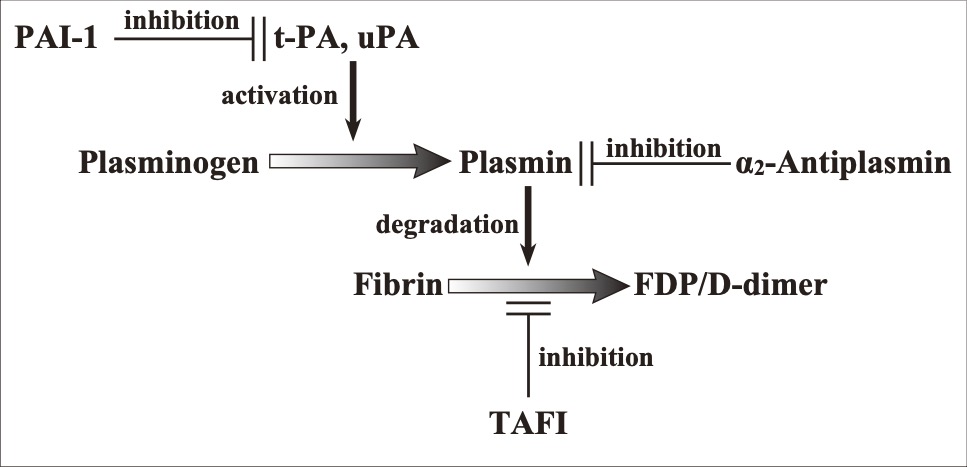
線溶反応とは線維素(フィブリン)溶解反応の略で、主にプラスミンがフィブリンを分解する反応(フィブリン分解)ですが、フィブリノゲンの分解をする場合もあります。またプラスミンは細胞外マトリックスなども分解し、増殖因子の活性化にも関与しており、組織修復や腫瘍細胞の浸潤などに関連しています。この反応は主に細胞表面で起きるため、細胞性線溶と呼ばれます。プラスミンのみならず、好中球エラスターゼもフィブリン分解に関与する場合もあり、このようなプラスミン以外のプロテアーゼによるフィブリン分解も線溶反応と呼ぶ場合もあります。このように線溶反応とは幅広い現象を含む反応です。
線溶反応に関する用語が必ずしも適切には使用されていない場合を見かけます。そのためいくつかの用語についてその意味をはっきりさせておく必要があります。
1. フィブリン分解とフィブリノゲン分解
プラスミンがフィブリンを分解する反応がフィブリン分解であり、フィブリノゲンを分解する反応がフィブリノゲン分解です。生理的条件下では、プラスミノゲンはフィブリン上で効率良く活性化されプラスミンとなり(→ 【プラスミノゲン活性化機構】、【t-PAによるプラスミノゲン活性化】)、生成されたプラスミンはフィブリン上では不活化を受けにくく(→【線溶反応の時間的・空間的制御】)、フィブリン表面を移動しながらフィブリンを分解します。一方、プラスミノゲンは流血中では活性化されにくく(→ 【プラスミノゲン活性化機構】)、またフィブリン表面上に存在するプラスミンが流血中に遊離しても速やかに不活化されるため(→【線溶反応の時間的・空間的制御】)、プラスミンが流血中のフィブリノゲンを分解することはほとんどありません。
一方、プラスミンの制御因子であるα2-アンチプラスミンが低下している病態(→【α2-アンチプラスミン低下と時間的・空間的線溶制御の破綻】)では、フィブリン表面から流血中に遊離したプラスミンが十分には不活化されず、特に線溶系の著しい活性化のために消費性にα2-アンチプラスミンが低下している線溶制御不能状態では、流血中に遊離するプラスミンの量も多くなるため、フィブリノゲン分解が惹起され、低フィブリノゲン血症を合併する場合があります。
フィブリン分解とフィブリノゲン分解は同時に起こり得る現象で、実際の臨床検査所見で明確に分類することは困難です。フィブリン分解の場合、分解されるフィブリンが凝固第XIII因子によって架橋された安定化フィブリンであれば、D-ダイマーが上昇することになります。一方フィブリノゲンからはD-D構造を持つ分解産物は産生されません。したがってD-ダイマーが上昇している場合はフィブリン分解が惹起されていると判断することができます。一方フィブリンの中でも凝固第XIII因子による架橋を受ける前の不安定フィブリンや、フィブリンがファンデルワールス力で重合するる前のフィブリンモノマーからはD-ダイマー以外のフィブリン分解産物(FDP)が産生されます。このFDPはフィブリノゲン分解でも産生されますが、フィブリノペプチドなど一部の構造が異なると論理的には推察されます。現在の市販されているでは、これらの違いを判別することはできません。このためフィブリノゲン分解が起こっているかどうかをFDPを用いて判定することは困難です。線溶制御不能状態に陥り、低フィブリノゲン血症を合併し、抗凝固療法や抗線溶療法などによって改善するような場合にフィブリノゲン分解が惹起されているかどうかの推察が可能なレベルです。
2. 一次線溶と二次線溶
線溶系の重要な活性化因子である組織プラスミノゲンアクチベータは、血栓形成による虚血などの刺激によって血管内皮細胞などから産生されます。このように血栓形成に反応して二次的に活性化された線溶反応を二次線溶と呼びます。一方、血栓形成とは関連なく活性化される線溶反応を一次線溶と呼びます。一次線溶はAL-アミロイドーシスなどで認められます(→文献)。この場合は詳細な機構は不明ですが、ウロキナーゼがその病態形成に関与しています。一次線溶は前立腺癌などウロキナーゼ産生腫瘍でも起こり得ますが(→文献)、多くの場合、凝固系の活性化を合併するため二次線溶も同時に起こっています。臨床的には一次線溶と二次線溶は同時に起こり得る病態であり、両者を明確に区別することやその関与の程度を評価することは困難です。
時に「一次線溶」=「フィブリノゲン分解」、「二次線溶」=「フィブリン分解」と記載されているものを見かけますが、これは明らかな誤りです。「一次線溶・二次線溶」は線溶活性化機構での分類(Inの段階の分類)であり、「フィブリン分解・フィブリノゲン分解」は線溶反応の基質の段階での分類(Outの段階の分類)です。このため、一次線溶でもフィブリン分解が惹起される場合もあり、また二次線溶でもフィブリノゲン分解が惹起される場合があります。
3. 線溶亢進と線溶抑制
このような表現もしばしば目にしますが、概念としては誤りとまでは言えないまでも、臨床的には的外れな言葉です。線溶反応が二次線溶の場合、線溶開始因子である組織プラスミノゲンアクチベータがフィブリン血栓に応じて産生され、またフィブリンを一種の補酵素として使用しているため、フィブリンの量に応じて線溶活性化の程度が決まります(フィブリン量が多ければ強い活性化が、少ないなら弱い活性化が惹起されます)。このため線溶活性化には適切な活性化状態が存在し、「亢進」とか「抑制」は、この「適切な」活性化を指標として評価しなければなりません。甲状腺機能異常症を考えてみると明らかで、「甲状腺機能亢進症(亢進状態)」と「甲状腺機能低下症(抑制状態)」の間には適切な甲状腺機能状態(euthyroidism)が存在します。線溶活性化の指標のPAPなどが上昇しているのは「活性化」が起きているだけであり、「亢進」しているかどうかは不明です。概念としては「亢進」や「抑制」はあり得ますが、日常診療において線溶系の活性化が「亢進」しているのか「抑制」されているのかの判断はほぼ不可能です。またこのような臨床に基づかないDICの分類も適切とは言えません。
狭義の線溶反応(フィブリン血栓の溶解反応)は、主に組織プラスミノゲンアクチベータによって開始されます。組織プラスミノゲンアクチベータは一本鎖の状態で、血栓による虚血刺激などで血管内皮細胞などから放出されますが、酵素前駆体である一本鎖の状態でも酵素活性を持っています。プラスミンなどによって活性化され二本鎖になると酵素活性が10倍上昇しますが、一本鎖の状態でもフィブリンと結合するとその酵素活性が上昇します。また基質であるプラスミノゲンも流血中では、閉じた形をしているため活性化されにくいのですが、フィブリン上では活性化されやすい状態になります。このため線溶系の活性化はフィブリン表面上で効率よく進行します。
止血血栓の溶解の場合、線溶反応の中心となるプラスミンの多くは組織プラスミノゲンアクチベータによって活性化されます。その活性化はフィブリン上で速やかに進行する一方、流血中での活性化は限定的です(→【プラスミノゲン活性化機構】、【t-PAによるプラスミノゲン活性化】)。生成したプラスミンはクリングルドメインにあるリジン結合部位を介してフィブリンのC-端リジン残基と結合します。またプラスミンがフィブリンを分解すると、新たなC-端リジン残基が出現し、この新たなC-端リジン残基を足場としてフィブリン表面上を移動しながら、分解していきます。一方、流血中に遊離したプラスミンはα2-アンチプラスミンにによって速やかに不活化されるため、通常、プラスミンは流血中ではその酵素活性を発揮することはありません。このように線溶反応はフィブリン表面で開始され進行する「空間的に制御」されています。
またフィブリン表面の線溶反応も、その活性化に重要な組織プラスミノゲンアクチベータはプラスミノゲンアクチベータインヒビターによって、ダイナミックに制御されていますし、プラスミンそのものも、凝固第XIII因子を介してフィブリンに固相化されたα2-アンチプラスミンにによって、適宜制御されています。このような機構によって線溶反応は適切な速度でフィブリンを分解するように「時間的な制御」も受けています。
線溶系の制御因子であるα2-アンチプラスミンにが低下し、線溶系の制御が十分に行うことができない病態を「線溶制御不能状態」と呼んでいます。この病態では、線溶反応(プラスミンによるフィブリン分解)の制御能が低下しており。その結果、適切な速度によるフィブリン分解が行われず、損傷部の治癒が十分に行われる以前にフィブリン血栓が分解されることになります。このフィブリン早期分解が起きると出血を呈することになります。これは線溶反応の「時間的制御の破綻」であり、臨床的には一旦止血は認められるものの、しばらくして出血が認められる再出血という症状を呈することになります。特にoozingと呼ばれる、滲み出るような出血を呈することが特徴とされていますが、ひどい場合には止血そのものがはっきりしない場合も経験します。「線溶亢進」なる病態はこの線溶制御不能状態と混乱しているのではないかと思います。線溶系の活性化が著しくともα2-アンチプラスミンにが保たれている状態では、フィブリン早期分解による出血傾向はまれです。
| |||||||||||||||