![]()
生体の力学的現象を扱うバイオメカニクス、特に細胞に加わる力学的刺激とその刺激に対する細胞の感知・応答機構に焦点を当てた研究を行っています。研究の主題は血流に起因する力学的刺激であるシェアストレス(shear stress)とそれが作用する血管内皮細胞の関係を探ることです。このことは血流を介した血管系システムの制御機構の解明に役立つだけでなく、血流依存性に起こる血管の新生、成長やリモデリングあるいはヒトの粥状動脈硬化症や動脈瘤の発生といった臨床医学的に重要な問題の解明にも繋がります。研究方法は培養した内皮細胞に流体力学的に設計した流れ負荷装置で定量的な shear stress を作用させて細胞応答を観察する独自の生体工学的実験を用いています。
- Shear stress の感知と情報伝達機構
- Shear stress による細胞の分化誘導
- Shear stress による遺伝子発現制御機構
1. Shear stress の感知と情報伝達機構
Shear stress の大きさを細胞内カルシウム濃度に変換する P2X4 プリノセプター
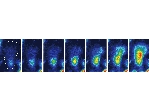
内皮細胞が shear stress を感知して、その情報を細胞内部に伝達する機構に関して、セカンドメッセンジャーである Ca2+ を介する情報伝達経路がある。ヒト血管内皮細胞に ATP 作動性カチオンチャネルの P2X4 受容体が優勢的に発現し(Am J Physiol 2000)、それが流れ刺激で起こる Ca2+ 流入に中心的な役割を果たし、shear stress という物理的な大きさを細胞内 Ca2+ 濃度に変換するトランスデューサーとして機能することことが判明した(Circ Res 2000)。
Shear stress 依存的に放出する ATP が P2X4 を活性化する
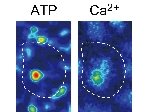
さらに shear stress による P2X4 の活性化には、流れ刺激によって放出される内因性の ATP が必要であり(Am J Phsiol 2003)、内因性 ATP の放出反応に、細胞膜カベオラ・ラフトに存在する FoF1ATP 合成酵素が関わっていることが判明した(Am J Physiol 2007)。最近、独自に開発した ATP のイメージング技術を用いて、流れずり応力による内皮細胞からの ATP 放出がカベオラから起こり、同じ局所でP2X4 受容体を介するカルシウムシグナリングが発火することを明らかにした(J Cell Sci 2011)。
Shear stress は細胞膜の物理的性質を変化させる
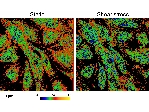
以上の結果から、 shear stress のメカノセンシング機構として細胞形質膜の物理的性質が shear stress により変化し、それが様々な膜分子の活性化を引き起こす可能性が考えられた。そこで、培養血管内皮細胞にシェアストレスを作用させたときの細胞膜リン脂質-水系の構造(lipid order)の変化と膜流動性の変化を解析した所、シェアストレスを作用させると即座に細胞膜のlipid orderが減少し、膜の流動性が増加した。この変化は内皮細胞だけでなく、人工脂質二分子膜で構成されるジャイアントリポソームでも同様に観察されたことから、物理現象であることが証明された(J Cell Sci 2013)。更に、細胞膜流動性を減少させると、shear stress 依存的な ATP 放出が抑制されることを明らかにした。細胞膜流動性の変化は様々な膜分子を活性化することが知られており、シェアストレスによる膜流動性の変化が内皮細胞のメカノトセンシングに重要な役割を果たすことを示唆する。
P2X4 プリノセプターは循環機能調節に関与する
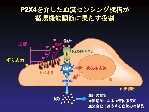
P2X4 を介する shear stress のセンシング機構が生体に及ぼす作用を確認する為、P2X4 遺伝子の欠損マウスを作製した。このマウスの内皮細胞では shear stress による Ca2+ 流入反応が起こらずNO産生が抑制されていた。さらに、血流増加による血管拡張反応が障害され全身の血圧が上昇していた。また、血流を減少させたときに生じる血管のリモデリングも障害を受けていた。このことから、P2X4 は血流刺激の情報を伝達するセンサー分子で、循環系の生理的な調節に重要な役割を果たしていることが示された(Nature Medicine 2006)。
2. Shear stressによる細胞の分化誘導
血管内皮前駆細胞(EPC)や胚性幹(ES)細胞が血行力学因子である shear stress や cyclic strain に反応して血管細胞へ分化することを明らかにした。
Shear stress による細胞の分化誘導
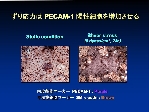
ヒトの末梢血を流れる EPC が shear stress に応答して増殖能が亢進し、内皮細胞への分化と管腔形成が促進することを観察した(J Appl Physiol 2003)。また、shear stress が血管内皮増殖因子受容体を活性化して、マウスの ES 細胞を内皮細胞へ分化誘導する効果があった(Am J Physiol 2005)。
さらに、shear stressがEPCやES細胞において動脈内皮のマーカーである ephrinB2 の発現を増加させる反面、静脈内皮マーカーである EphB4 の発現を抑制することから、shear stress が内皮の動静脈分化にも影響を及ぼすことを示し(J Appl Physiol 2009, Arterioscler Thromb Vasc Biol 2009)、胚の発生時における血管形成に shear stress が重要な役割を果たしていることを示唆した。
Cyclic strain による細胞の分化誘導
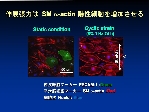
一方、cyclic strain 刺激がES細胞を平滑筋細胞へ分化誘導し、その効果に血小板由来増殖因子受容体のリン酸化が関わっていることを明らかにした(J Appl Physiol 2008)。
ハイブリッド型人工血管への応用

このことを応用し、微細孔構造を持つポリマー管にES細胞を播種し、拍動性の shear stress と cyclic strain を同時に与えることで、内皮細胞と平滑筋細胞の二層構造を持つ生体の血管組織に近いハイブリッド型人工血管の開発を行うことができた(J Artif Organs 2005)。
3.Shear stress による遺伝子発現制御機構
Shear stress による遺伝子発現変化

Shear stress が内皮細胞の遺伝子の発現を転写調節あるいは転写後調節することを明らかにした。既知の遺伝子だけでなく、多くの未知の遺伝子も shear stress に感受性のあることを mRNA の differential display 法で示し(BBRC 1996)、さらに DNA マイクロアレイ解析により遺伝子全体の約3%(約600の遺伝子に相当)が shear stress に応答することを観察した(J Atheroscler Throm 2003)。また、shear stress の感知に関与する P2X4 受容体の発現が shear stress で抑制を受けるが、これは転写因子 SP1 が関連した転写抑制に基づくことを明らかにした(Am J Physiol 2001)。
層流と乱流の shear stress による遺伝子発現制御機構の違い
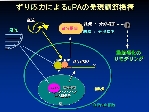
また、病態発生と関連して、動脈硬化巣は血流が乱流の部分に好発することが知られているが、遺伝子に対する shear stress の作用が層流と乱流で異なることを明らかにした。動脈硬化の発生に関与するウロキナーゼ型のプラスミノーゲン・アクチベータ(uPA)の遺伝子の発現は層流で低下し、乱流で増加した(Am J Physiol 2004)。この結果は乱流刺激により動脈硬化が形成する事実を支持する。その機構は層流では転写因子 GATA6 を活性化し転写を抑制するとともに mRNA の分解速度を速める効果が認められた。一方、乱流では転写には影響せず、mRNA の安定化を起こす作用が確認された。
内皮細胞だけでなく、肝細胞においても shear stress が PAI-1(プラスミノーゲン・アクチベータ阻害因子)の遺伝子の転写を活性化し、その遺伝子の発現を調節することが示された(Am J Physiol 2006)。.
Shear stress と cyclic stretch による遺伝子発現の違い
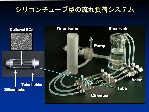
研究室で開発したシリコンチューブ型流れ負荷装置による検討で内皮細胞における NO 合成酵素(eNOS)とエンドセリン(ET-1)の遺伝子の応答が shear stress と cyclic strain の同時負荷と各々の単独負荷では異なることを観察した(J Biotechnol 2008)。
 HOME
HOME 研究内容
研究内容 発表論文・業績
発表論文・業績 メンバー
メンバー Link
Link