研究
臨床薬理学分野は、臨床でサイエンス力を発揮できる薬剤師を養成することを目標としています。当分野教授は薬剤部長を併任していることから、配属学生は最先端の薬物治療を多く学ぶことができます。また、臨床で生じる問題を抽出し研究テーマにすることで、患者さんに還元できる研究を実践しています。
薬剤師が臨床業務を行う際に求められる能力は、研究を遂行する際に必要とされる能力と多くの共通点があります。当分野では、研究を通じて「基礎的・汎用的能力」「論理的思考力」「問題解決能力」などをしっかりと教育します。また、学生個々の研究能力を引き出す目的で、自発的な研究計画の立案・考察を推奨し、議論を活発に行っています。研究成果が出た際は、積極的に学会・論文発表が出来るよう全面的にサポートします。
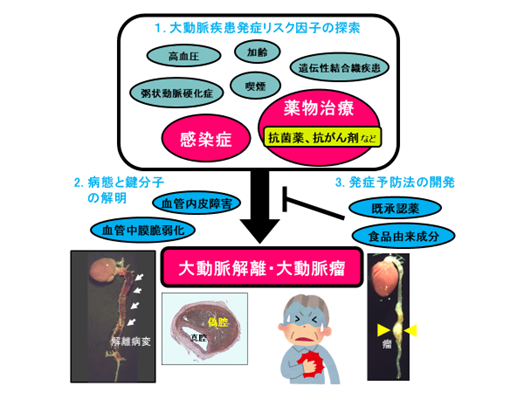
急性大動脈解離発症の引き金となる因子を探り、予防戦略確立を目指す
急性大動脈解離は、私たちの体の中で最も太く大きな血管である「大動脈」の壁が裂け、激烈な痛み、主要な血管分枝の閉塞、そして血管の破裂による大量出血などをきたし、突然死の原因となる重篤かつ緊急性の高い疾患です。男性、高齢者、喫煙歴のある方、高血圧患者さんなどで発症率が高いと言われています。また、遺伝性の結合織疾患を罹患しておられる方では大動脈解離などの血管疾患が発症しやすいことが知られています。近年、これまで知られていた前述のリスク因子に加え、薬物治療の有害事象として発症する例が報告されたり、感染症を契機として発症する可能性が疑われています。そこで私たちのグループでは、医療ビッグデータ解析の手法により、急性大動脈解離発症の引き金となるかもしれない様々な因子について、その関連性を検証しています。さらに私たちの確立した「薬剤誘発性大動脈解離易発症モデルマウス」を用いて、解離発症のメカニズム解明や、発症予防に有効な物質の探索など、予防戦略確立に向けた研究を行っています。
参考文献
- Kondo M, Izawa-Ishizawa Y, Goda M, Hosooka M, Kagimoto Y, Saito N, Matsuoka R, Zamami Y, Chuma M, Yagi K, Takechi K, Tsuneyama K, Ishizawa K. Preventive Effects of Quercetin against the Onset of Atherosclerosis-Related Acute Aortic Syndromes in Mice. Int. J. Mol. Sci. 2020;21(19):7226.
- Izawa-Ishizawa Y, Imanishi M, Zamami Y, Toya H, Nagao T, Morishita M, Tsuneyama K, Horinouchi Y, Kihira Y, Takechi K, Ikeda Y, Tsuchiya K, Yoshizumi M, Tamaki T, Ishizawa K. Development of a novel aortic dissection mouse model and evaluation of drug efficacy using in-vivo assays and database analyses. J. Hypertens. 2019;37(1):73-83.
- Imanishi M, Izawa-Ishizawa Y, Sakurada T, Kohara Y, Horinouchi Y, Sairyo E, Zamami Y, Takechi K, Chuma M, Fukushima K, Ikeda Y, Fujino H, Yoshizumi M, Tsuchiya K, Tamaki T, Ishizawa K. Nitrosonifedipine, a Photodegradation Product of Nifedipine, Suppresses Pharmacologically Induced Aortic Aneurysm Formation. Pharmacology. 2018;102(5-6):287-299.
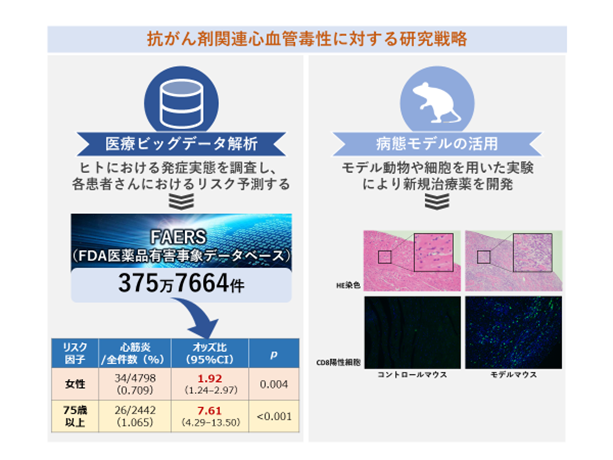
データサイエンスを駆使した薬剤性心血管毒性のリスク評価と治療法開発
近年、様々な抗がん剤の開発によって、がん患者の生命予後は改善傾向にあります。一方で、抗がん剤治療によりがんは治癒したにも関わらず、心血管障害の発現によりかえって生命予後が悪化してしまう患者さんがいることが問題となっています。そのため、抗がん剤関連心血管毒性の克服は、がん患者の生命予後改善を目指すうえで大きな課題であると言えます。
私たちは、この問題に対して、データサイエンスと臨床薬理学の研究手法を活用して取り組んでいます。1000万症例を超える電子カルテデータベースや副作用報告データベースなどの医療ビッグデータを解析することで、実臨床における心血管毒性の発症実態を明らかにし、 どのような患者さんで心血管毒性が起こりやすいのかを調査しています。さらに、抗がん剤関連心血管毒性のモデルマウス等を用いた実験により、新規治療薬の探索を進めています。このように、抗がん剤関連心血管毒性のリスクを評価し、その発現を予防すること、そして起こってしまった心血管毒性に対して有効な治療を実施することで、抗がん剤関連心血管毒性の克服を目指しています。
参考文献
- Zamami Y, Niimura T, Okada N, Koyama T, Fukushima K, Izawa-Ishizawa Y, Ishizawa K: Factors Associated With Immune Checkpoint Inhibitor-Related Myocarditis. JAMA Oncol. 2019; 5(11): 1635-1637.
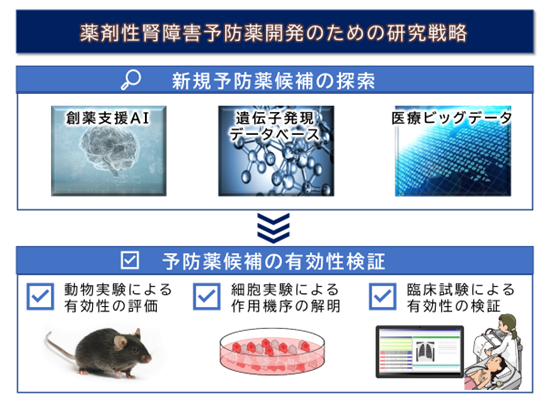
ビッグデータ解析を活用した薬剤性腎障害予防薬の開発
高齢化に伴い、がん患者は増加の一途をたどっています。さらにがん薬物療法の進歩に伴いがんサバイバーの増加も報告されており、今後もがん化学療法を受ける患者数が増加し続けることが予想されています。一方でがん化学療法施行時には、悪心・嘔吐、腎障害、脱毛などの有害事象が高頻度に起こり、患者のQuality of life (QOL)は著しく低下します。中でも、抗がん剤による薬剤性腎障害のコントロールは、患者のQOL向上、治療継続、予後改善のための重要な課題です。しかし、2016年に日本腎臓学会等により発表された「がん薬物療法時の腎障害診療ガイドライン2016」において腎障害の予防に推奨される薬剤はなく、ハイドレーションなどの現状の予防法では、完全に腎障害を抑えることはできないため、新たな予防薬の開発が求められています。
そこで本研究では、実臨床を反映する医療ビッグデータ、さらに創薬支援AIや遺伝子発現データベースなど複数のデータベース解析を活用して抗がん剤による薬剤性腎障害に対して予防効果を有する可能性が高い医薬品の抽出を試みています。さらに、抽出された候補医薬品に関して、動物実験、細胞実験などの基礎実験、カルテ調査などの臨床研究を行い、予防薬の有効性の検証及び作用機序解明を行い、候補医薬品の腎障害予防薬としての臨床応用を目指します。
参考文献
- Kanda M, Goda M, Maegawa A, Yoshioka T, Yoshida A, Miyata K, Aizawa F, Niimura T, Hamano H, Okada N, Sakurada T, Chuma M, Yagi K, Izawa-Ishizawa Y, Yanagawa H, Zamami Y, Ishizawa K: Discovery of preventive drugs for cisplatin-induced acute kidney injury using big data analysis. Clin. Transl. Sci. 2022; 15(7): 1664-1675.
- Goda M, Kanda M, Yoshioka T, Yoshida A, Murai Y, Aizawa F, Niimura T, Zamami T, Hamano H, Okada N, Yagi K, Chuma M, Izawa-Ishizawa Y, Ishizawa K: Effects of 5-HT3 receptor antagonists on cisplatin-induced kidney injury.Clin. Transl. Sci. 2021; 14(5): 1906-1916.
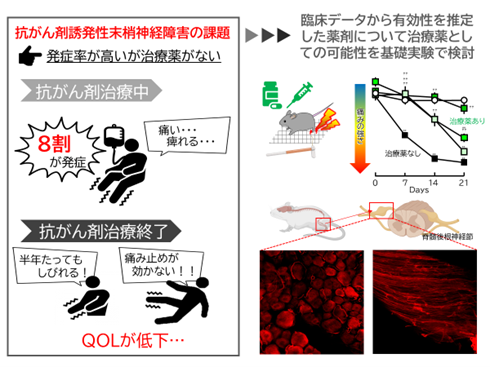
抗がん剤による末梢神経障害の克服を目指した既承認薬の応用研究
がん薬物療法の発展によって、がんは不治の病ではなく治療によって共生する慢性疾患へと変化し、がんと共に健やかな生活を送るには、がん治療で生じる種々の苦痛を取り除くことが必要です。抗がん剤によって生じる末梢神経障害は、抗がん剤治療患者の約80%が経験するといわれています。末梢神経障害は繰り返しの抗がん剤治療で難治化し、半年以上にわたるしびれや痛みが出現することで日常生活に支障をきたします。しかしながら、このような症状は通常の痛み止めは効果が弱く、抗がん剤治療の中止以外に症状を抑えられる有効な手立てがありません。薬には治療効果をもたらす主作用とそれ以外の副作用があります。「副作用」という文字だけで考えるとネガティブな印象がありますが、別の角度から考えると、まったく別の疾患に治療効果をもたらす作用なのかもしれません。本研究では、臨床データを基に、オキサリプラチンやパクリタキセル使用時に生じる末梢神経障害に対する有効性を持つ薬剤を臨床現場から拾い上げ、基礎・行動薬理学的観点から、しびれや痛みを抑制する作用機序の解明を進めることで、既に活用されている薬剤から新しい薬理作用を発見し、治療薬を開発するための研究を行っています。
参考文献
- Zamami Y, Niimura T, Kawashiri T, Goda M, Naito Y, Fukushima K, Ushio S, Aizawa F, Hamano H, Okada N, Yagi K, Miyata K, Takechi K, Chuma M, Koyama M, Kobayashi D, Shimazoe T, Fujino H, Izawa-Ishizawa Y, Ishizawa K: Identification of prophylactic drugs for oxaliplatin-induced peripheral neuropathy using big data. Biomed. Pharmacother. 2022; 148: 112744.
最適ながん治療環境の構築を目指した網羅的な要因探索
分子標的治療薬(TKI)の登場により、がん治療は大きく進歩しました。慢性骨髄性白血病はその最たる疾患であり、TKIにより長期生存が見込めるようになり、がんとの共生が可能な疾患の1つとなりました。そのため、がんサバイバーの抱える問題にも目を向けられるようになり、その問題の1つに再発の問題があります。現状では寛解した患者さんであってもTKIを休薬すると過半数以上が再発してしまうため、一生涯継続してTKI服用しなければなりません。10年以上の長期にわたるTKI治療を受けている患者さんも増えてきており、長期投与による様々な副作用の発現も大きな問題です。また、TKIは非常に高価な薬剤であるため、高額な薬剤費による患者さんの経済的な負担も大きく、経済的な理由は薬物治療のアドヒアランスが低下する要因の1つです。また、がん患者はがん治療薬以外にも非常に多くの非常に多くの支持療法薬を使っていますが、1つ1つの支持療法薬の使用が治療効果にどの程度の影響があるのかということについて、がん治療薬ごとには十分な検証がされていません。そこで、データベース研究、臨床研究および基礎研究など様々な手法を駆使することで、最大の治療効果を得るための新たな方策を探索しています。新たな治療標的・治療薬や支持療法薬はもちろんですが生活習慣や食生活など多様な因子を含めて様々な方法からアプローチを行い、臨床現場に還元できるエビデンスの創出を目標に研究を行っています。

参考文献
- Yagi K, Mitstui M, Zamami Y, Niimura T, Izawa-Ishizawa Y, Goda M, Chuma M, Fukunaga K, Shibata T, Ishida S, Sakurada T, Okada N, Hamano H, Horinouchi Y, Ikeda Y, Yanagawa H, Ishizawa K: Investigation of drugs affecting hypertension in bevacizumab-treated patients and examination of the impact on the therapeutic effect. Cancer Med. 2021; 10: 164-172.
- Yagi K, Shimada A, Sendo T: Pharmacological inhibition of JAK3 enhances the antitumor activity of imatinib in human chronic myeloid leukemia. Eur. J. Pharmacol. 2018; 825: 28-33.

