登録の手順 〜研究に参加される医師の方へ〜
各施設での試験開始までの手続き
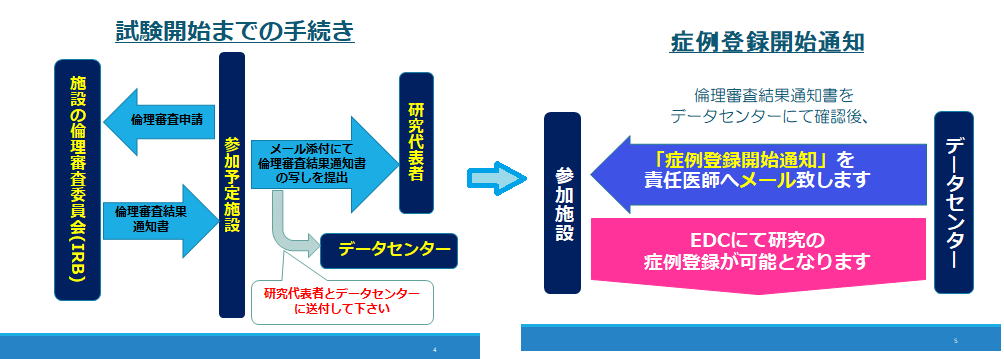
①各施設で、本研究への参加について、ご施設の規定に則り倫理審査委員会(IRB)へご申請をお願い
いたします。
②倫理審査委員会に承認され、倫理審査結果通知書が届きましたら、原本を施設保管し、写しをメール添付にてJRAP事務局(研究代表者)とデータセンターへご提出をお願いいたします。
③書類内容を確認したのち、登録開始できるようにシステムのセットアップを行います。
④倫理審査の内容を確認しEDCの設定終了後、参加施設の責任医師へメールにて「症例登録開始通知」
連絡を送信します。この連絡をもって、ご登録が可能となります。
IRB/倫理委員会審査へ申請するための必要書類
・AEDs-PG実施計画書
・AEDs-CH実施計画書
・同意説明文書
・研究代表施設倫理委員会判定通知書
上記の書類はJRAP事務局を通じて入手できます。事務局(下記)までお問い合わせください。
なお倫理委員会を持たないクリニックなどのご施設は、参加申請に関しましてJRAP事務局までお問い合わせください。
JRAP事務局
〒420-8688
静岡県静岡市葵区漆山886 静岡てんかん・神経医療センター内
E-mail jrap.office@gmail.com
TEL.054-245-5446
FAX.054-247-9781
症例登録方法
「症例登録開始通知」メールに記載してあるURLより、症例登録を行います。必要な情報をデータセンターに入力します。
登録内容の詳細は「症例登録開始通知」メールが届いた段階で、事務局よりご案内いたします。
お問い合わせ
JRAP事務局
〒420-8688
静岡県静岡市葵区漆山886 静岡てんかん・神経医療センター内
E-mail jrap.office@gmail.com
TEL.054-245-5446
FAX.054-247-9781