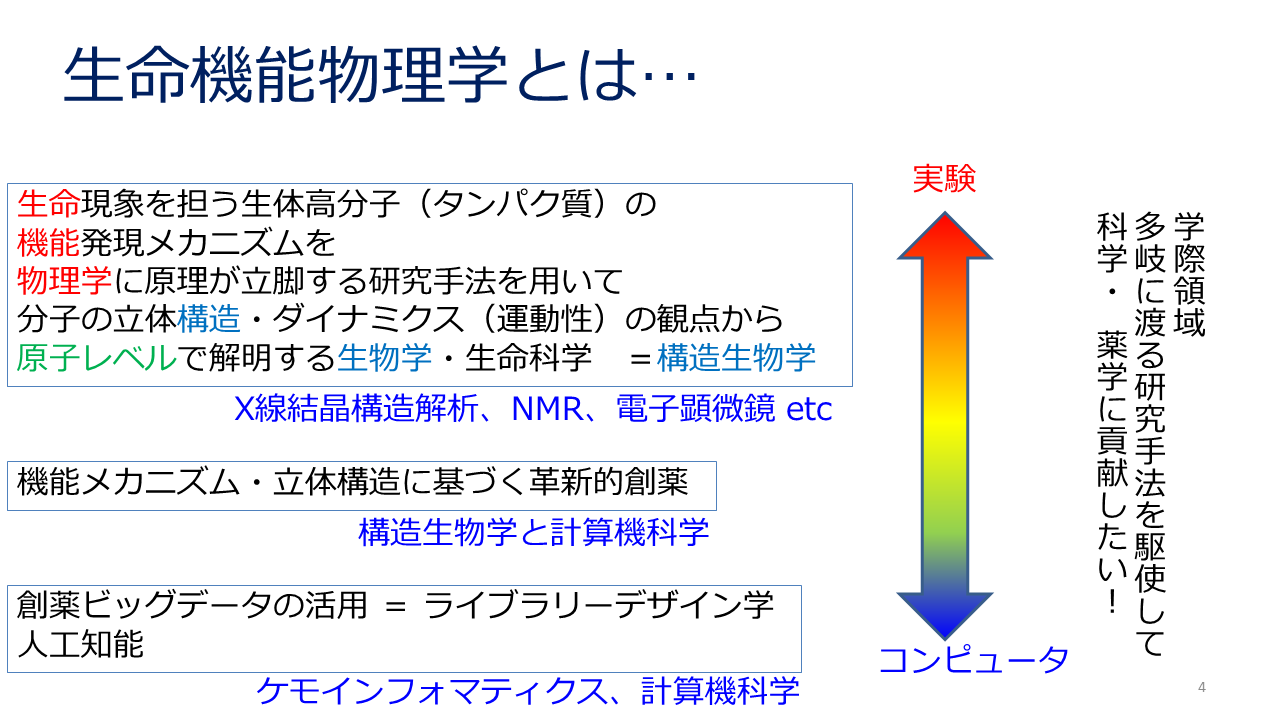
当講座について
生命機能物理学講座は、「様々な生命現象を担う生体高分子(主にタンパク質)の 機能がどのようなメカニズムで生じるのかを、核磁気共鳴(NMR)法やX線結晶解析を中心とした物理化学的な解析手法により、原子レベ ルで解明する」ことを目標にしています。 現在、研究の対象としているタンパク質(関連する疾病・治療薬)は、電位依存性イオンチャネル(不整脈、疼痛、糖尿病、乾癬、アレルギー、不妊治療)、トランスポーター(薬剤耐性、高脂血症)、ウイルス由来タンパク質(ウイルス感染)、タンパク質の翻訳因子群(がん、細胞増殖、幹細胞、ウィルス感染)など非常に多岐に渡っています。 これらのタンパク質は、各種リガンドの結合、膜電位の変化、脂質二重膜中の微量脂質との相互作用などにより、立体構造や運動性が変化します。それによって、タンパク質の機能が変調を受け、正常な生理機能を発現し、また、機能不全や過剰亢進があれば疾病へと繋がります。 このからくり(メカニズム)を原子分解能で知ることができれば、タンパク質のどの部位にどのような形の化合物を結合させればよいか、といった創薬戦略を構築することが出来ます。さらに、実際に化合物の探索・構造最適化研究へと展開します。
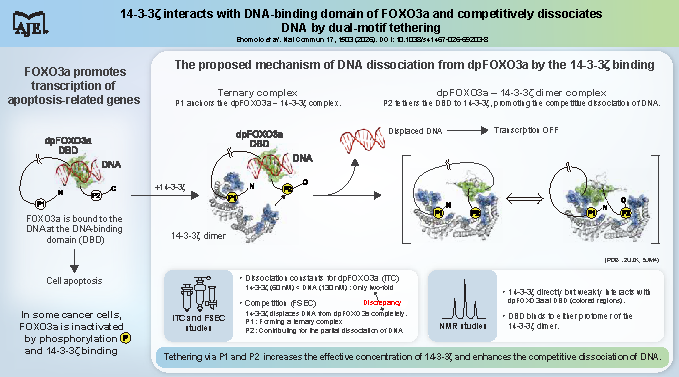
最近の研究より:14-3-3ζタンパク質によるがん抑制因子FOXO3aの機能阻害機構の解明
がんは日本の死因第1位であり治療法の確立が求められています。がん細胞では、様々なタンパク質が恒常的にリン酸化され、正常細胞とは異なるタンパク質間相互作用(PPI)を形成することで、がんの悪性化を引き起こします。したがって、がん悪性化に関与するPPI機構を立体構造の観点より明らかにし、特異的に阻害する化合物を見出すことができれば、新規抗がん剤の創製につながります。本研究では、本来はがんを抑制するはずの転写因子FOXO3aが、がん細胞ではリン酸化と14-3-3ζの結合によりDNAから解離して機能を失うことに注目し、FOXO3aと14-3-3ζの結合様式とDNA解離機構を解明しました。具体的には、NMRなどの生物物理学的手法を用いて、14-3-3ζがFOXO3aのリン酸化モチーフでのテザリングを利用して結合力を増大させ、さらにDNA結合部位とも直接結合してDNAを競合的に解離させる巧みなPPIと競合メカニズムを初めて実証しました。(Enomoto S. et al. Nat. Commun. 2026, 慶應プレスリリース, 慶應英文ニュースレター”The Penmark", 研究紹介YouTube)