KOMP2 (Knockout Mouse Phenotyping Program) and IMPC (the International Mouse Phenotyping Consortium) Annual Fall Meetingに参加して
中村卓郎(公益財団法⼈がん研究会・がん研究所)
2019 年11 ⽉17 ⽇〜19 ⽇に⽶国メリーランド州ロックヴィルで開催されたKOMP2 & IMPC Annual Fall Meetingに出席し、国外におけるマウスモデルの作製・解析の実情に接した。世界規模の遺伝⼦変異マウスモデルのコンソーシアムの活動状況について報告する。
IMPC は、世界各地24 箇所の研究機関から成るコンソーシアムで、遺伝⼦改変マウスを作製しターゲッティングコンストラクトやES 細胞を保存するとともに、そのフェノタイプを解析して情報の共有を図ることを⽬的としている。我が国からは理化学研究所バイオリソース研究センターがメンバーとして参加している。KOMP2はNIHの傘下であるNational Human Genome Research Institute (NHGRI)によるプログラムで、IMPC と協同しながら活動を⾏っているが、メンバーはオーバーラップしている。
今回のミーティングには IMPC のメンバー機関を中⼼に 13 か国から約 100 名の参加者があった。主なテーマは、IMPC の変異マウス作製と解析の現状、⽼化、haploinsufficiency による胎⽣致死効果、⼼⾎管系と代謝の異常、マイクロビオーム、形態解析、⾏動解析と感覚機能解析、オミックス解析、アウトリーチ活動、など⾮常に多岐にわたる発表と討論があった。活動の⼀部を紹介すると、2018〜19 年でコンソーシアムとして 1025 の新しい変異マウスを作製したが、その⼤部分は CRISPR/Cas9 を使ったゲノム編集技術によるものであった。IMPC 発⾜以来の合計としても 8572 ラインの 40%をゲノム編集による変異系統が占める状況となっている。胎⽣致死となる変異系としては、2016 年以来で 979 ラインが作製された。IMPC として、フェノタイプ解析の共通プロトコールを⽤いており、胎児、成体でそれぞれ厳密に管理されたパイプラインで評価を⾏うことで、研究施設間でのバイアスを極⼒減らす努⼒がされている。
我々の⾏っている⽀援プログラムとは予算スケールや運営システムが異なるのは当然だが、⽬的が異なることに注意したい。先端モデル動物⽀援プラットフォームでは、⽀援を希望する研究者(以下ユーザー)の依頼の下、作製や解析が⾏われるのに対して、 IMPC の事業ではコンソーシアムメンバーが⾃主的に改変したい遺伝⼦を決定する。ユーザーの希望というものはなく、ここではユーザーは既に遺伝⼦改変されたES 細胞やコンストラクトを有償で⼊⼿する。ただし、⼤規模な事業であり、近い将来にはタンパク質をコードする全ての遺伝⼦について⼀通りの遺伝⼦改変モデルが完成される⾒込みなので、多くの研究者の希望に対応が可能かも知れない。実際、我々のプラットフォームでもIMPC で⼊⼿可能な変異コンストラクトがあれば、その利⽤を推奨している。IMPC のリソースは全世界で使⽤されており、2019 年にはこのリソースを⽤いた論⽂数が2073編に及んだ。
コンソーシアム⾃⾝が改変する標的を決めることはユニークな取り組みも⽣み出している。Olfactory receptors, TMEM, RIKEN cDNA, Family with sequence similarity, solute carrier, zinc finger protein 等に代表される、現状では殆ど機能が分かっていない⼤規模なファミリー遺伝⼦を体系的に変異させる計画も検討されている。
個々の機関からの発表や提案で興味深かったものを、幾つか紹介する。カリフォルニア⼤デイヴィス校のDr. Lloyd らは、30 系統のKO マウスの成体メタボロミクスの解析を⾏い糖代謝や⾎管病変などの多くのフェノタイプが性依存的であることを⽰した。コネティカット⼤のDr. Rowe は新しいゲノム編集技術として、2種類のRNA エンドヌクレアーゼ(Cas9-Cpf1 及びCas9-Cas12)を使った、より正確なエクソンターゲッティングの成績を紹介した。ベイラー⼤のDr. Heaney は、ヒトの遺伝⼦の15%に当たる3000 遺伝⼦が⽚アレルの機能⽋失で重篤なフェノタイプが出ることを報告し、コンソーシアムにおける今後の重要な検討課題であるとの意⾒共有をみた。ドイツのヘルムホルツセンターのDr. Galter らは、マウスのX 線イメージの解析に機械学習を導⼊し、⾻格異常の⾃動解析系を⽴ち上げている。
⽣命科学連携推進協議会の各プラットフォームも、⽇本分⼦⽣物学会を初めとする各種の学術団体の会合で展⽰と紹介を⾏っているが、IMPC も世界各地の学会において年間約10カ所でプレゼンや展⽰ブースの設置を⾏っている。特にアメリカ⼈類遺伝学会(ASHG)、ヨーロッパ⼈類遺伝学会(ESHG)とは強いコラボレーションを毎年⾏なっている。ここでは、遺伝病に対する研究リソース側からの⽀援という⽴場から⼩児の遺伝病患者を対象としたプログラムにも積極的な参加を⾏なっていることが注⽬された。
⼀⽅、前述のように我々の⽀援プラットフォームが「ユーザーの提案ありき」で運営されているのに対し、IMPC は⾃⾝の研究計画の下で活動を⾏っている。したがって、当然のことながらIMPC の所属機関単独或いは複数の所属機関の活動から独⾃の論⽂が作成されている。例えば、IMPC によるヒト疾患モデル(Cacheiro et al., Mamm Genome, 2019)はIMPC の最新の活動状況と具体的なモデルの紹介をした論⽂であるが、各国のES細胞⽣産状況をまとめた解説やCas9によるオフターゲット効果の論⽂もNat Genet誌に投稿予定とのことであった。また、マウスの糞便のマイクロビオーム解析では遺伝⼦変異よりも施設間の変化の⽅が著しかったことなど、多施設共同研究ならではの研究結果も取りまとめ中である。
今回の会議でIMPC における盛んな独⾃研究成果を⽬の当たりにして、我々の⽀援活動に対するヒントになったことであるが、⽀援側研究者に対するインセンティブが重要な課題として提起されていることに対して、プラットフォームを構成する拠点の連携による独⾃の研究を実施することは⼀つの解決策ではないかと思われた。従来のユーザーが主導する研究論⽂の共著者として名前を連ねるインセンティブとは異なり、拠点に所属する研究者の独⾃の業績になるだけではなく、⽀援活動の質の⾼さを明⽰することにもなる。実施に当たっては、予算の問題、あくまでも⽀援担当者の⾃主性が尊重されること、⽂部科学省の⾒解も確認する必要があることなど課題も多いが、⼀度検討されるべき点ではないかと考える。
IMPC のメンバーには、年間変異マウス50 系統以上の作製が義務付けられ、⾦額的な負担もあるなどもともかく、対象は原則的に研究機関であることを想定しているため、我々のプラットフォームがメンバーとして参加することは現実的ではないが、マウスモデルの作製と解析の最新の情報発信源として何らかのコンタクトを続けていくことは重要であると考える。最後に、貴重な機会を与えて頂いた⽣命科学連携推進協議会の皆様に深謝致します。

IMPC 科学委員⻑のDr. Steve Brown (左、MRC Harwell)とNHGRI のDr. Colin Fletcher(右)によるイントロ
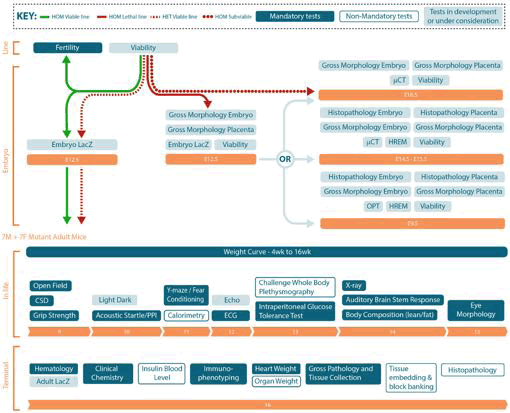
胎児及び成体マウスのフェノタイプ解析パイプライン。⾼度かつ系統的なフェノタイプ解析が実施されている。







