LTB4 結合実験 ( 五十嵐 敏雄 )
第二生化マニュアル目次
(1) レセプター標品の調整 ( 材料; 豚白血球の場合)
【 豚白血球の調整 】
1) 豚血液 10L に CPD 液 1L を混ぜる。
cf. CPD; 0.26M citrate, 0.37M trisodium citrate, 0.4M dextrose
2) 豚血液 10L に対し 2L の 6% dextran ( 0.9% NaCl含 )を加え、 室温に30分間
放置して赤血球を沈降させ、デカンテーションと吸引で上清を回収する。
3) 上清を centrifugation. 200×g for 10min
4) 0.75% NH4Cl + 16.5mM Tris-HCl + 1mM EDTA ( pH 7.4 )
1L で沈殿を susupend し、室温に 30分間静置して溶血させる。
5) centrifugation. 200×g for 10min
6) 沈殿を PBSで suspend し、cfg. 200×g for 10min で洗浄する。
7) 1011個のオーダーで、白血球を採取出来る。
【 膜画分の調整 】 (以下は 4℃で行う)
1) centrifugation. 200×g for 10min
2) 沈殿を buffer(A)で懸濁し、(B)も加えて 300ml にする。 cf. 108~109 cell/ml
(A) 20mM Tris-HCl + 0.25M Sucrose + 10mM MgCl2 + 1mM EDTA (
pH 7.4 )
(B) final conc. 0.5mM PMSF , 2mM DTT
3) 超音波処理で細胞を破壊する。
振動子は直径約 2cm のもの。条件 preset 20, pulse 4, output 5 で 2回行う。
住友の50ml チューブに20ml ずつ分注して行うとよい。
4) 超音波処理後、2)と同量の PMSF を再度加える。
5) centrifugation. 800×g for 15min
6) 5)の沈殿は buffer(A)で 再懸濁した後、(B)を加えて 240ml にし、
3) と同じ条件で超音波処理を行う。3)で破壊されなかった白血球が破壊される。
5)に戻って centrifugation. 800×g for 15min 、上清を 5)の上清と一緒にする。
7) 5)の上清を centrifugation. 8,000×g for 15min ( 7,200rpm SAKUMA
M160-4 )
沈殿としてミトコンドリア画分を分別除去出来る。
8) 7)の上清、約470ml を supercentrifugation 130,000×g ( 40,000rpm )
for 90min
roterは RP45T-367 を用い、94PA tube に 70ml×6 本 で分注するとよい。
9) 上清を除去し、沈殿を buffer (A)で 懸濁して150ml にする。
10) supercentrifugation 130,000×g ( 40,000rpm ) for 90min
roterは RP45T-367 を用い、94PA tube に 70ml×2 本 で分注するとよい。
11) 上清を除去し、沈殿を buffer (A)で懸濁して 100ml にする。
膜画分として約150mgを得る。-80℃で数カ月保存することが出来る。
【 可溶化画分の調整 】
1) 下記の濃度を充たし、蛋白質濃度 が 1mg/ml となるように膜を希釈調整する。
20mM Tris-HCl + 10% Sucrose + 10mM MgCl2 + 2mM EDTA + 2mM DTT
+ 0.5mM PMSF + 1μM GDP + 0.15M NaCl + CHAPS 0.2% ( final )
2) 空気をアルゴンガスで置換後、30分間 ROTATOR でゆっくりと撹拌処理する。
これで 0.15M NaCl と 0.2% CHAPS の処理により表在性の蛋白質を除去出来る。
3) supercentrifugation 130,000×g ( 40,000rpm ) for 90min
roterは RP45T-367 を用い、94PA tube に 70ml×4 本 で分注するとよい。
4) 沈殿をヒスコトロンを用いて1) と同じ容量の溶液 (C) に懸濁する。
(C) 50mM Tris-HCl + 10mM MgCl2 + 2mM EDTA + 2mM DTT
+ 0.5mM PMSF + 1μM GDP + CHAPS 0.5%
5) 空気をアルゴンガスで置換後、30分間 ROTATOR でゆっくりと撹拌処理する。
0.5% CHAPS により LTB4R 画分が可溶化される。
6) supercentrifugation 130,000×g ( 40,000rpm ) for 90min
roterは RP45T-367 を用い、94PA tube に 70ml×4 本 で分注するとよい。
7) 上清、約30mg を可溶化画分として回収出来る。-80℃で数カ月保存可能。
(2) 結合実験
【 試薬 】
1) 結合実験用緩衝液 ( 反応液 )
50mM Tris-HCl ( pH 7.4 ) + 10mM MgCl2 + 10mM NaCl
膜で特にガラス容器を使用する場合、0.1% BSA を加えるとよい。
2) 標識リガンド ( [3H]LTB4 )
[5,6,8,9,11,12,14,15-3H(N)]-, メタノール溶液 ( Dupont )
50nM なので、反応液で 50倍に希釈し、1nM にする。
3) 非標識リガンド ( cold LTB4 )
LTB4 のメタノール溶液を反応液で希釈し、4μM にする。
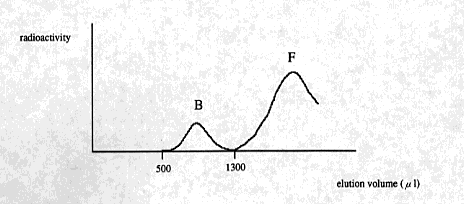
4) B/F 分離用品 ( B;リセプターと結合したリガンド F;フリーのリガンド )
・膜画分の場合; Whatman GF/C フィルター cf. filteration technique
・可溶化画分の場合; NAP-5 (Pharmacia) cf. gel-filtration assay
5) カラム洗浄/保存液 0.5M NaCl + 20% EtOH
6) カラムの平衡化及び溶出用バッファー
50mM Tris-HCl ( pH 7.4 ) + 10mM MgCl2 + 10mM NaCl + 0.01% CHAPS
【 結合実験 (膜画分の場合) 】
1) プラスチック製の試験管 (容積 5ml 以上) に
☆ 反応液 50μl, ☆ 反応液 または cold LTB4 50μl, ☆ [3H]LTB4 50μl
を入れて、25℃で 3分間、プレインキュベーションする。
2) サンプルも 25℃で 3分間、プレインキュベーションする。
3) 1) の試験管に 2) のサンプル 50μl を混ぜて
25℃ で 1時間インキュベーションする。( 反応系 ; 200μl )
4) 氷冷した反応液 2ml を加え、反応を停止させた後、GF/C フィルターを通して
吸引濾過する。free なLTB4 はフィルターを素通りするが、膜成分は素通りし
ないため、レセプターに結合した [3H]LTB4 はフィルターにトラップされる。
5) 氷冷した反応液 2ml でフィルターを 4 回洗浄する。
6) フィルターを 60℃で一時間乾燥する。
7) フィルターにシンチゾールEX-Hを 3ml 加え、放射活性を測定する。
付記) 測定サンプルが多数ある場合
丸底96穴プレートで上記1)~3)のように反応させた後、96穴GF/C フィルター
に吸着させ、50℃で一時間乾燥後、専用のシンチゾールを25μl を加えて、
TOP-COUNT で測定することが出来る。
【 結合実験 ( 可溶化画分の場合) 】
1) エッペンドルフチューブ に
☆反応液 50μl, ☆ 反応液 または cold LTB4 50μl, ☆ [3H]LTB4 50μl
を入れて、25℃で 3分間、プレインキュベーションする。
2) サンプルも 25℃で 3分間、プレインキュベーションする。
3) 1) のチューブに 2) のサンプル 50μl を混ぜて
25℃ で 1時間インキュベーションする。( 反応系 ; 200μl )
4) 1分間 on ice で反応を停止させた後、全量をピペットで回収し NAP-5 に通す。
NAP-5 は予め上記の平衡化及び溶出用バッファーで平衡化しておく。
5) NAP-5 にさらに溶出用バッファー 300μl を通し、4) 及び 5) で溶出される
最初の 500μl は破棄する。
6) さらに溶出用バッファー 800μl を通し、溶出される液を回収する。
レセプターと結合した LTB4 は大きな分子となるので、ここで溶出される。
7) シンチゾールEX-Hを 3ml 加え、放射活性を測定する。
8) NAP-5 はカラム容積の 3倍量の洗浄/保存液で洗い、2回程、再利用出来る。
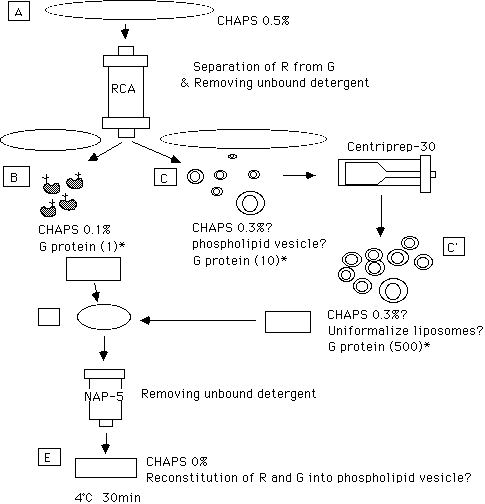
【 結合実験 ( RCA 吸着画分以後の場合) 】
1) RCA 素通り画分 50ml を Centriprep-30 による遠心濃縮 (3,000 rpm,30min)
4~5回繰返しにより RCA 素通りの濃縮画分 約1 ml (50倍濃縮)を作成する。
この画分には RCA 吸着画分の約500倍 G 蛋白質が含まれ、リン脂質も多く、
リポソームの形成が予想される。 ( Ar で置換して -80度で数カ月保存出来る。)
2) RCA 吸着画分 450μl と RCA 素通りの濃縮画分 50μl を mix する。(体積比9:1)
3) その直後、mix 500μl を反応液に buffer change ( NAP-5 で )しCHAPS 除去。
30分間 4℃で放置すると LTB4R はリポソーム上で G 蛋白質と再構成される。
4) その後の結合実験は可溶化画分の場合と同様に行うことができる。
第二生化マニュアル目次

